На этой странице вы найдете все материалына сайте из нескольких разделов, сгруппированные по дате публикации. Мы благодарим вас за то, что нашли время заглянуть сюда.

Обновление информации по клиническим исследованиям компании «Новартис» в области СМА
Компания Новартис предоставила свежую информацию по клиническим исследованиям своего препарата Бранаплам, предназначенного для терапии спинальной мышечной атрофии. Бранаплам (LMI070) — пероральный препарат, который увеличивает количество функционального белка SMN, продуцируемого геном SMN2 (белок SMN поддерживает двигательные нейроны, которые контролируют активность мышц).
Дефекты в клеточной «системе очистки» могут являться причиной болезней двигательных нейронов
Нарушения в естественной системе очистки наших клеток – она называется аутофагия – могут быть причиной развития болезней двигательных нейронов, таких как спинальная мышечная атрофия (СМА), – предполагают исследователи из Университета Вюрцбурга в Германии.

Компания Цитокинетикс объявила результаты клинических испытаний 2-й фазы препарата релдесемтив у пациентов со спинальной мышечной атрофией
Первое исследование мышечно-направленной терапии у пациентов со СМА показало потенциально клинически значимое влияние на дистанцию, пройденную в ходе 6-минутного теста и максимальное давление на выдохе.
Ситуация с лечением Спинразой (Нусинерсеном) в Европе и в России (по данным компании Biogen на июнь 2018 г.)
Американская фармацевтическая компания Biogen, которая разработала и выпустила на рынок единственное на сегодняшний день лекарство для лечения больных спинальной мышечной атрофией (СМА) Nusinersen (торговое наименование
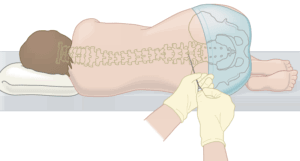
Как проводится люмбальная пункция?
Люмбальная пункция (или поясничный прокол) обычно проводится для диагностики (когда нужно проанализировать состав спинномозговой жидкости пациента) или с лечебной целью, когда препарат нужно доставить непосредственно

Компания Roche выпустила обновление информации по своим исследовательским программам в области СМА
В настоящее время компания Roche проводит клинические исследования препарата RG7916, модификатора сплайсинга SMN2, повышающего уровень белков SMN.
Компания AveXis набирает пациентов со СМА 2-го типа в программу STRONG клинического исследования препарата AVXS-101
Ключевые критерии включения в тестирование:
— Возраст до 60 месяцев (5 лет) на дату начала исследования и подтвержденный во время скрининга генотип болезни, выраженный в способность сидеть без посторонней помощи в течение 10 или более секунд; способность стоять или ходить отсутствует;

Компания Roche допускает возможность участия российских пациентов в программе Sunfish
Фармацевтическая компания Roche выпустила обновленную сводку по своим исследованиям в области СМА, где упоминает ситуацию с закрытием набора пациентов на исследование Sunfish и описывает вариант возможности участия в нем российских пациентов. .

Компания Roche завершила набор в программу Sunfish: россияне в нее не попадают
Компания Roche объявила о завершении набора пациентов со всего мира для участия в программе Sunfish клинического исследования препарата RG7916 для пациентов со СМА 2-го и 3-го типов.

30 июня мы участвуем в «Московском фестивале волонтеров»
Этим летом наш фонд впервые принимает участие в ежегодном «Московском фестивале волонтеров», который проходит уже в четвертый раз. Он состоится 30 июня на открытом воздухе

Открыт набор пациентов со СМА1-го типа в программу исследования препарата RG7916
Мы рады сообщить, что в России открылся первый центр клинических исследований препаратов для больных спинальной мышечной атрофией, и теперь у российских семей есть возможность попасть в программу клинических исследований СМА в своей стране.
Центр открыт в Москве, на базе НИКИ педиатрии имени Ю. Е. Вельтищева, и сейчас ведется набор пациентов со СМА 1-го типа возрастом до 7 месяцев для участия в исследовании Firefish препарата RG7916 компании Roche.

Школа СМА в Екатеринбурге! Итоги
Друзья, хотим рассказать вам о том, как проходила наша трехдневная майская Школа СМА в Екатеринбурге. В первый день мы провели семинар для команды паллиативного отделения

Компания Roche останавливает исследовательскую программу по препарату Олезоксим
Фармацевтическая компания Roche распространила официальное сообщение о закрытии своей программы по разработке препарата Олезоксим (olesoxime), предназначенного для терапии СМА.
Обновление по программе клинических исследований препарата Бранаплам компании Новартис
Бранаплам — это пероральный препарат, находящийся в разработке на 1\2 фазе клинических исследований, основной целью исследований на этой фазе является оценка безопасности и эффективности препарата у пациентов со СМА 1 типа.
Авексис начал набор участников в клиническое исследование пресимптоматических младенцев со СМА возрастом до 6 недель
Лечение СМА пациентов настолько рано насколько это только возможно — критически важно, т.к. позволяет спасти мотонейроны до того, как они будут навсегда утрачены.

Круглый стол «Судьба пациентов с разными типами СМА»
Приглашаем сотрудников и волонтеров НКО на Круглый стол «Судьба пациентов с разными типами СМА (спинальной мышечной атрофии)». На Круглом столе мы обсудим механизм заболевания, варианты

Круглый стол «Новая терапия и клинические исследования для СМА»
15 мая с 16 до 19 мы приглашаем сотрудников НКО для обсуждения темы новых терапий и клинических исследований в области СМА. За последние несколько лет

Упростили процедуру принятия решений по установлению инвалидности
В России упростили процедуру принятия решений по установлению инвалидности и сроках освидетельствования. Согласно текущей версии документа диагноз «спинальная мышечная атрофия» (СМА) относится к категории заболеваний,

