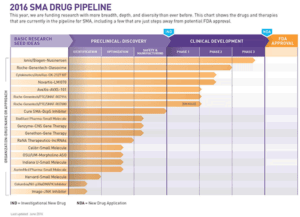
Cure SMA представила данные по ведущимся клиническим исследованиям в области лечения СМА
Помимо финансирования части исследований, Cure SMA взяли на себя обязательство выступать в интересах пациентов при участии в разработке лекарственных средств. Это необходимо для того, чтобы внутренние регулирующие органы лучше понимали потребности сообщества пациентов со СМА.