
В статье, подготовленной на основе доклада «Новые возможности лечения СМА: от мышц к мотонейронам» кандидата медицинских наук, генетика и невролога Сергея Александровича Курбатова, кратко рассказывается о механизмах патогенетической терапии и перспективных подходах к лечению спинальной мышечной атрофии.
Сколько в мире редких генетических заболеваний?
В настоящий момент известно более 8000 редких (орфанных) заболеваний, суммарно частота которых выше, чем совместная распространенность онкологических заболеваний и СПИДа. В 80 процентах случаях орфанные заболевания обусловлены повреждением известных генов и становятся причиной смерти почти 30 процентов умерших детей на первом месяце жизни. Больные с орфанными заболеваниями требуют стационарного лечения и занимают до 10 процентов больничных коек в год. В 65 процентах случаев орфанные заболевания приводят к укорочению продолжительности жизни и значительно снижают качество жизни.
Если говорить только о наследственных нейромышечных заболеваниях (НМЗ), то описано более тысячи отдельных нозологических единиц, из них как минимум 100 форм с поражением мотонейронов. Из этих почти ста форм до 95 процентов случаев приходится на СМА 5q.
Колоссальный успех медицины и исследований последних лет состоит в том, что найдены новые подходы к патогенетической терапии и лечению НМЗ и в первую очередь для СМА 5q, и исследования в этой области продолжаются.
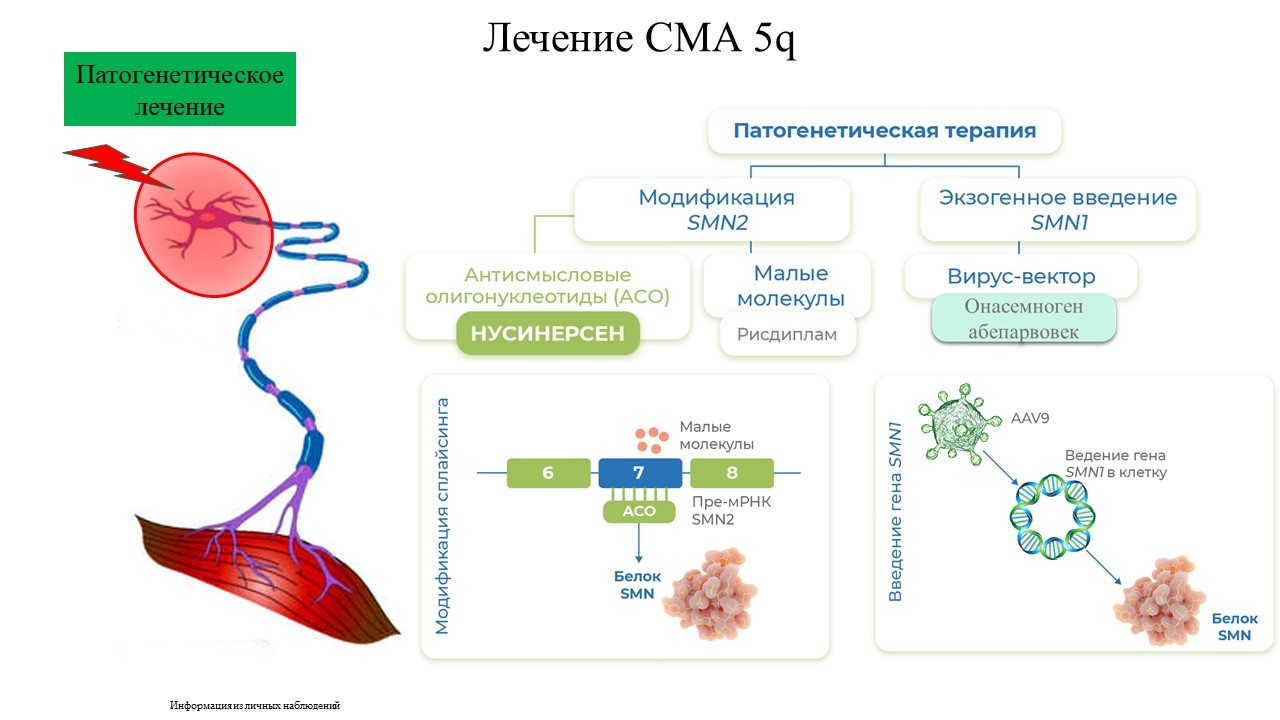
В настоящее время патогенетическая терапия при СМА 5q направлена на сохранение мотонейронов и предотвращение их гибели путем увеличения количества белка выживаемости мотонейронов (SMN). Увеличение количества SMN достигают разными подходами с использованием антисмысловых олигонуклеотидов (Нусинерсен) или малых молекул (Рисдиплам) которые модифицируют сплайсинг РНК гена SMN2, а так же вирус-векторной доставкой синтетического функционального гена SMN1 (Онасемноген абепарвовек).
Механизм развития и возникновения СМА
Напомню, что мотонейроны обеспечивают широкий спектр функций для обеспечения нормального функционирования движения, в том числе иннервацию, трофику и сокращение мышечных волокон скелетной мускулатуры.
При СМА 5q уменьшение количества белка SMN приводит к постепенной потери мотонейронов и последующей деннервации мышечных волокон, их атрофии и гибели. Оставшиеся в живых мотонейроны пытаются сохранить соседние мышечные волокна погибших мотонейронов и работают с огромной перегрузкой. Неуклонная гибель мотонейронов приводит к появлению основных симптомов в виде слабости, мышечных атрофий, нарушения дыхания и глотания и в конечном итоге к летальному исходу.
Патогенетическая терапия при СМА 5q способна обеспечить достаточную выработку белка SMN и остановить гибель мотонейронов, в итоге мотонейроны потенциально способны брать под контроль все новые мышечные волокна, однако достаточное увеличение мышечных волокон по ряду причин не происходит при SMA 5q.
Восстановления утраченных мышц вследствие заболевания практически не происходит.
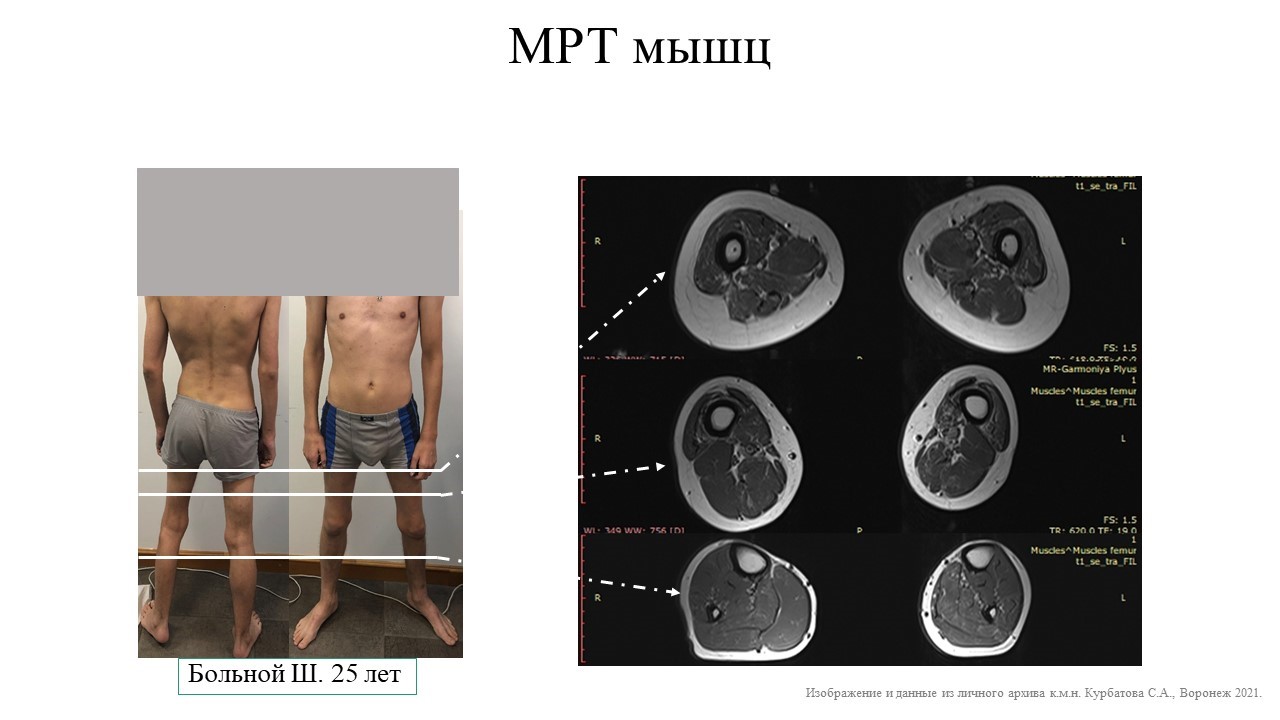
Если на момент начала патогенетической терапии есть значительная атрофия мышц, как на представленном рисунке (диффузная атрофия мышц бедер, кроме длинной приводящей и короткой мышцы бицепса бедра, и атрофия мышц задней группы мышц левой голенени), то одобренное лечение может замедлить процесс атрофий, но почти не сможем вернуть ему те мышцы, которые уже утрачены. Лечение сохраняет мотонейроны, приводит к более стабильной и эффективной их работе, однако не приводит к появлению новой мышцы взамен погибшей.
Можно ли восстановить погибшие мышцы у человека со СМА?
При атрофии скелетных мышц, сохранение мотонейронов не позволяет полностью восстановить потерю двигательной активности с использованием одобренной патогенетической терапии. Разрабатываются новые подходы к лечению СМА 5q направленные на восстановление утраченных мышц и увеличение объема мышечных волокон. На международном конгрессе Myology 2022 в Ницце представлены десятки успешных экспериментальных работ:
- в том числе на животных по трансплантации скелетных мышц напечатанных на 3D принтере
- клинических исследований на пациентах со СМА 5q на примере снижение активности белка миостатин, приводящих к увеличению объема скелетных мышц
- по выявлению точек приложения для ингибирования атрофии и старения (саркопении) мышц
- по активации асимметричного деления миобластов с восстановлением погибших мышц
- по активации механизмов повышающих силу и эффективность сокращения сохранных мышц
В одной из работы предварительны предварительные результаты клинического исследования MANATEE (NCT05115110) по снижению активности миостатина в сочетании с применением малых молекул (Рисдиплам) свидетельствуют в пользу лучшей эффективности относительно монотерапии малыми молекулами.
Не вызывает сомнение, что воздействие на разные точки приложения позволяющие увеличить количество синапсов, мышечных волокон, коллатералей аксонов, сосудистую сесть, силу сокращения мышечных волокон и другие механизмы нервно-мышечного комплекса смогут привести к повышению двигательной активности у людей со СМА 5q.
Атрофия мышц не только при гибели мотонейронов
Мышцы могут атрофироваться не только у пациентов со СМА 5q. Если человек стареет, болен раком, диабетом, миопатией или мышечной дистрофией, то его мышцы начинают атрофироваться, хотя мотонейроны при этом не повреждаются.
Описано множество причин, запускающих процесс атрофии мышц. Один из таких механизмов преждевременного старения и атрофии мышц провоцируется широким спектром заболеваний связан с активацией сигнального пути Notch2 (избыточно вырабатывается растворимый Dll4 эндотелиальными клетками капилляров) в результате мышца уменьшается в объеме, начинается преждевременная атрофия и гибель мышечных волокон. Тропониновый комплекс — другой важный белковый комплекс скелетной мышцы. Неонатальная форма белка устойчива к гипоксии и может развить бОльшую силу сокращения, в отличии от взрослой формы, однако к году неонатальная замещается на взрослую форму.
Рассматриваются подходы к изменению пропорции в тропониновом комплексе с увеличением неонатальной формы и увеличению силы сокращения мышцы.
Несомненно, в скором времени появиться широкий спектр лекарственных препаратов позволяющих влиять на патологические механизмы с разными точками приложений, которые будут усиливать процессы регенерации, трофики и работы мышц.
Эти же механизмы с учетом специфики могут помочь пациентам со СМА 5q на фоне основного патогенетического лечения, способствовать увеличения сила, объема и трофики мышц.
Подводя итоги. С некоторой долей условности процессы, происходящие в организме
пациента со СМА 5q, можно сравнить со строительством домов. Мотонейрон – это поврежденный «кран», который можно отремонтировать/сварить, но он не сможет работать на полную мощность и его нужно беречь от больших нагрузок. Однако есть строители, строительные лифты, веревки и другие приспособления, которые практически не задействованы при нормальной работе «крана», и при правильной организации работы могут разгрузить поврежденный «кран», что будет незаметно поломки. В организме так же множество резервных механизмов, так и со СМА 5q ученые ищут резервные пути для достижения терапевтических целей.
Благодарим Сергея Александровича Курбатова за медицинскую редактуру статьи.
Данный материал носит исключительно информационный характер и не является рекламой. Рекомендации относительно индивидуального применения лекарственных препаратов следует получать у вашего лечащего врача.




