Бранаплам — экспериментальный препарат для лечения СМА. В клинических исследованиях должны участвовать младенцы до 6 месяцев со СМА I. Препарат разрабатывает компания Новартис.
Бранаплам имеет механизм действия, схожий с ранее разработанным препаратом Спинраза. Он увеличивает в организме больного количество белка, дефицит которого приводит к возникновению и развитию СМА. Препарат вводится перорально (через рот).
Клинические исследования препарата
В августе 2018 года в России в Екатеринбурге (на базе Детской городской клинической больницы №9) открылся первый российский центр клинических исследований препарата. Пациенты, отвечающие определенным критериям, список которых можно посмотреть здесь, участвуют в международном клиническом исследовании. Всего в России Бранаплам исследуется на базе 6 центров.
Препарат Бранаплам исследуется на безопасность и эффективность в многоцентровом международном клиническом исследовании фазы 1\2 на пациентах со СМА 1 типа, в исследовании могли принять участие младенцы младше 6 месяцев на момент начала участия.
Клинические исследования препарата проводятся в нескольких центрах в разных европейских странах, а также в 6 центрах на территории России.
В июле 2019 года компания Новартис объявила о завершении набора участников клинического исследования.
В программу 2 части исследования включено 25 малышей со СМА 1 типа. Помимо набранной группы в 1 части исследования принимают участие 7 детей (из 13 изначально включенных в эту часть) — что позволяет говорить о накопленном опыте применения препарата от 3 до 4 лет для участников 1 части.
Данные, которые исследователи планируют получить по итогам исследования этой фазы позволят принять решение о последующих исследованиях препарата.
В ноябре 2020 года Компания Новартис сообщила, что продолжает клинические исследования препарата бранаплам (LMI070), перорального модулятора сплайсинга SMN2 c приемом препарата один раз в неделю.
Данный материал носит исключительно информационный характер и не может служить рекламой. Рекомендации относительно индивидуального применения этого лекарства следует получать у вашего лечащего врача.
Другие статьи о препарате Бранаплам
Последние публикации о лекарствах и клинических испытаниях
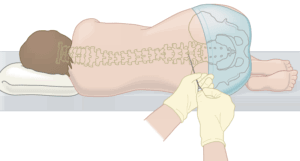
Как проводится люмбальная пункция?
Люмбальная пункция (или поясничный прокол) обычно проводится для диагностики (когда нужно проанализировать состав спинномозговой жидкости пациента) или с лечебной целью, когда препарат нужно доставить непосредственно

Компания Roche выпустила обновление информации по своим исследовательским программам в области СМА
В настоящее время компания Roche проводит клинические исследования препарата RG7916, модификатора сплайсинга SMN2, повышающего уровень белков SMN.
Компания AveXis набирает пациентов со СМА 2-го типа в программу STRONG клинического исследования препарата AVXS-101
Ключевые критерии включения в тестирование:
— Возраст до 60 месяцев (5 лет) на дату начала исследования и подтвержденный во время скрининга генотип болезни, выраженный в способность сидеть без посторонней помощи в течение 10 или более секунд; способность стоять или ходить отсутствует;

Компания Roche допускает возможность участия российских пациентов в программе Sunfish
Фармацевтическая компания Roche выпустила обновленную сводку по своим исследованиям в области СМА, где упоминает ситуацию с закрытием набора пациентов на исследование Sunfish и описывает вариант возможности участия в нем российских пациентов. .

Компания Roche завершила набор в программу Sunfish: россияне в нее не попадают
Компания Roche объявила о завершении набора пациентов со всего мира для участия в программе Sunfish клинического исследования препарата RG7916 для пациентов со СМА 2-го и 3-го типов.

Открыт набор пациентов со СМА1-го типа в программу исследования препарата RG7916
Мы рады сообщить, что в России открылся первый центр клинических исследований препаратов для больных спинальной мышечной атрофией, и теперь у российских семей есть возможность попасть в программу клинических исследований СМА в своей стране.
Центр открыт в Москве, на базе НИКИ педиатрии имени Ю. Е. Вельтищева, и сейчас ведется набор пациентов со СМА 1-го типа возрастом до 7 месяцев для участия в исследовании Firefish препарата RG7916 компании Roche.

