Бранаплам — экспериментальный препарат для лечения СМА. В клинических исследованиях должны участвовать младенцы до 6 месяцев со СМА I. Препарат разрабатывает компания Новартис.
Бранаплам имеет механизм действия, схожий с ранее разработанным препаратом Спинраза. Он увеличивает в организме больного количество белка, дефицит которого приводит к возникновению и развитию СМА. Препарат вводится перорально (через рот).
Клинические исследования препарата
В августе 2018 года в России в Екатеринбурге (на базе Детской городской клинической больницы №9) открылся первый российский центр клинических исследований препарата. Пациенты, отвечающие определенным критериям, список которых можно посмотреть здесь, участвуют в международном клиническом исследовании. Всего в России Бранаплам исследуется на базе 6 центров.
Препарат Бранаплам исследуется на безопасность и эффективность в многоцентровом международном клиническом исследовании фазы 1\2 на пациентах со СМА 1 типа, в исследовании могли принять участие младенцы младше 6 месяцев на момент начала участия.
Клинические исследования препарата проводятся в нескольких центрах в разных европейских странах, а также в 6 центрах на территории России.
В июле 2019 года компания Новартис объявила о завершении набора участников клинического исследования.
В программу 2 части исследования включено 25 малышей со СМА 1 типа. Помимо набранной группы в 1 части исследования принимают участие 7 детей (из 13 изначально включенных в эту часть) — что позволяет говорить о накопленном опыте применения препарата от 3 до 4 лет для участников 1 части.
Данные, которые исследователи планируют получить по итогам исследования этой фазы позволят принять решение о последующих исследованиях препарата.
В ноябре 2020 года Компания Новартис сообщила, что продолжает клинические исследования препарата бранаплам (LMI070), перорального модулятора сплайсинга SMN2 c приемом препарата один раз в неделю.
Данный материал носит исключительно информационный характер и не может служить рекламой. Рекомендации относительно индивидуального применения этого лекарства следует получать у вашего лечащего врача.
Другие статьи о препарате Бранаплам
Последние публикации о лекарствах и клинических испытаниях

Заявление компании Рош о поддержке пациентов в связи с конфликтом в Украине
10 марта компания Рош в официальном обращении пациентскому сообществу сообщила о продолжении поставок препарата рисдиплам для пациентов в России, а также об открытии специальной программы поддержки доступа к рисдиплам для украинских пациентов СМА, как в Украине, так и вынужденных покинуть страну.

Данные 6-12 месячного наблюдения пациентов в исследовании STRONG интратекального применения AVXS-101
Исследование СТРОНГ стартовало в конце декабря 2017 года. Оно было остановлено FDA в 2019 году после сообщения о находках в параллельных преклинических исследованиях, которые могли потенциально влиять на безопасность применения. После долгих проверок данных это ограничение было снято во второй половине 2021 года, однако прерванный набор в исследование СТРОНГ не возобновился. После снятия ограничений на проведение исследований AVXS-101 IТ (интратекального ввода) были запущены другие, новые программы клинических исследований IT-версии препарата.
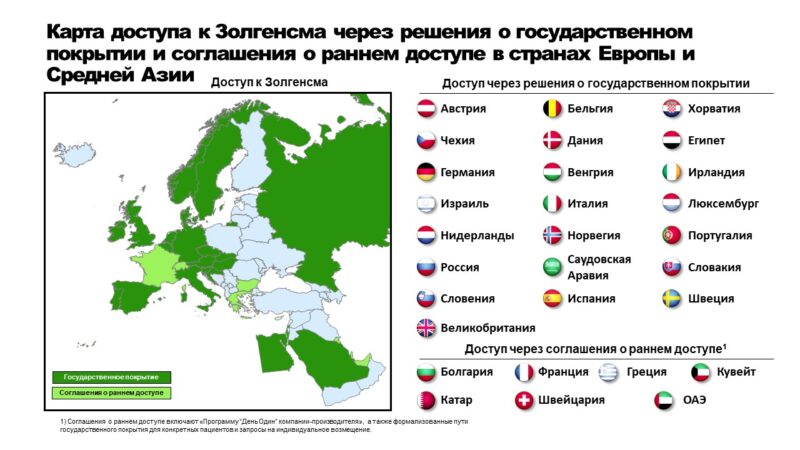
Доступ к Золгенсма в странах Европы и Средней Азии
В России препарат был одобрен в декабре 2021 года и оплачивается за счет средств федерального бюджета в рамках государственного фонда «Круг Добра».
Хирургия позвоночника эффективна у детей со СМА 1 типа, но не лишена рисков
Операция по исправлению кифосколиоза — сочетания двух типов аномального искривления позвоночника — позволяет успешно ввести Спинразу (нусинерсен) в позвоночный канал у детей со спинальной мышечной атрофией (СМА) 1 типа, как показывает исследование серии случаев.

Инструкция к препарату Онасемноген абепарвовек (Золгенсма)
Золгенсма (onasemnogene abeparvovec) — препарат генной терапии, разработанный для лечения больных проксимальной спинальной мышечной атрофией, вызванной нарушением в гене SMN1.

Инструкция к препарату Рисдиплам (Эврисди)
Рисдиплам (Эврисди) – препарат для лечения СМА, разработанный компанией Roche в сотрудничестве с PTC Therapeutics и SMA Foundation. Рисдиплам является модификатором сплайсинга (генетической модификации) гена SMN2, увеличивающим экспрессию полноразмерных функциональных белков.

