Компания Биоген представила новые данные по эффективности и безопасности применения Нусинерсен (Спинраза) у пресимптоматических пациентов со спинальной мышечной атрофией (СМА). Представленный анализ среза данных на февраль 2020 года и охватывает более 4,5 лет наблюдения, включая дополнительные 11 месяцев наблюдения в предыдущим обнародованным результатам. Предыдущий срез данных проводился в марте 2019 года и мы также публикуем его данные.
Данные получены из клинического исследования NURTURE, являющегося на сегодня самым длительным исследованием применения лекарственной терапии у пресимптоматических пациентов со спинальной мышечной атрофией. Новые результаты были представлены на прошедшей виртуальной Конференции Cure SMA Research & Clinical Care Meeting 10-12 июня 2020 года.
NURTURE — продолжающееся исследование фазы 2, открытое исследование 25 пресимптоматических пациентов, с генетически подтвержденным диагнозом СМА (наиболее вероятно разовьется СМА 1 или 2 типа), которые получили первую дозу нусинерсен в возрасте до 6 недель после рождения. Протокол исследования был продлен на дополнительные 3 года, чтобы дать возможность Biogen оценить долгосрочную эффективность и безопасность нусинерсен в течение 8 лет и на основе полученных данных лучше понять значение раннего лечения. Больше информации об исследовании вы можете найти на clinicaltrials.gov. (номер исследования (NCT02386553)
Новые данные покрывают практически год дополнительного наблюдения и показывают, что пресимптоматически получившие лечение SPINRAZA® (nusinersen) продолжают демонстрировать продолжительный результат от лечения. Максимальный период наблюдения покрывает 4.8 лет продолжающегося лечения нусинерсеном, 100% детей (25 patients), начавших лечение до появления первых симптомов болезни, живы и не нуждаются в постоянной вентиляции легких. Пациенты продолжают сохранять и прогрессивно набирать новые двигательные навыки по сравнению с естественным течением заболевания (без лечения). 96% сейчас могут самостоятельно ходить с поддержкой.
Все дети, которые достигли способности ходить самостоятельно (многие в тот же самый временной период развития, что и здоровые дети) сохраняют эту функцию с момента, когда она впервые была достигнута на момент последнего визита в исследовательские центры.
Нусинерсен хорошо переносился участниками исследования, без каких-либо дополнительных побочных эффектов в течение этого дополнительного срока наблюдения. Ни один ребенок не вышел из исследования по причинам перенесенных побочных реакций на препарат.
Дополнительные результаты из промежуточного анализа на февраль 2020 года:
- Все участники исследования, кто ранее научился ходить с поддержкой (92%) и ходить самостоятельно (88%) сохранили эту возможность в течение более чем 11 месяцев с момента последнего среза данных, предшествующего текущему.
- В течении этого, более чем 11 месяцев дополнительного наблюдения, 1 ребенок достиг возможности ходить с поддержкой (повысив процент до 96% во всей группе участников) и также достиг максимальной оценки по шкале CHOP-INTEND, повысив общее количество участников исследования, кто достиг максимальной оценки по этой шкале до 21 из 25 (84%).
- Пациенты с 2 копиями гена SMN2 также показали возможность оценки их двигательных функций по шкале Хаммерсмит (Hammersmith Functional Motor Scale Expanded scale (HFMSE), что нетипично для пациентов с этой формой не получающих лечение.
РАНЕЕ ОПУБЛИКОВАННЫЕ ДАННЫЕ (СРЕЗ НА МАРТ 2019 ГОДА)
? Исследование изучает (и продолжается на сегодня) работу Нусинерсен (#спинраза) у пациентов с генетически подтвержденным #СМА до момента проявления первых симптомов
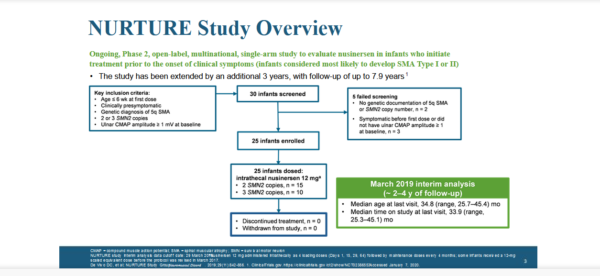
?В исследование включали пациентов с 2 или 3 копиями гена SMN2, т.е. наиболее вероятно разовьющими СМА1 или СМА2 типа соответственно
? И возрастом до 6 недель до начала терапии
?30 пациентов было скринировано (рассматривалось для включения в исследование)
?25 пациентов были включены в исследование (соответствовали критериям включения и не имели критериев исключения), из который 15 пациентов с 2 копиями и 10 пациентов с 3 копиями
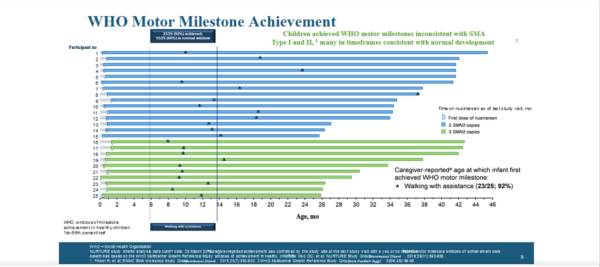
?Важно отметить, что 3 пациента не включенных в исследование не были включены из-за того, что за время скрининга (осмотров и подготовки к включению в программу) — проявились симптомы заболевания. Это подчеркивает важность МГНОВЕННЫХ мер, которые должны быть предприняты для лечения СМА, т.к. симптомы развиваются очень быстро.
?Представленные ниже данные — срез полученных результатов на 29 марта 2019 года
К этому периоду:
?Ни один из участников исследования не вышел из программы
? Средний возраст участников — 34,8 мес (медиана от 25,7 до 45,4 мес), т.е. средний возраст участвующих на дату среза от 2 до почти 4 лет
?Среднее время приема препарата — 33,9 мес (медиана от 25,3 до 45,1 мес), т.е. средний продолжительность лечения на этот срез от 2 до почти 4 лет
? Помимо сбора данных о безопасности и эффективности нусинерсен, в программе собираются данные об уровне нейрофиламентов и возможности использования этого параметра как потенциального индикатора возможных физических улучшений.
?РЕЗУЛЬТАТЫ
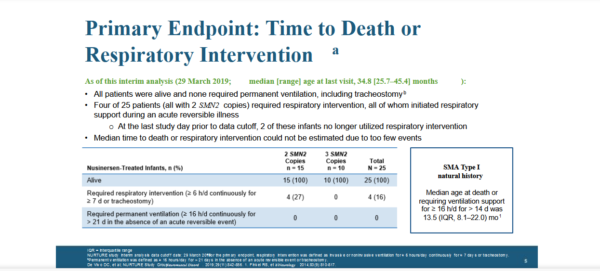
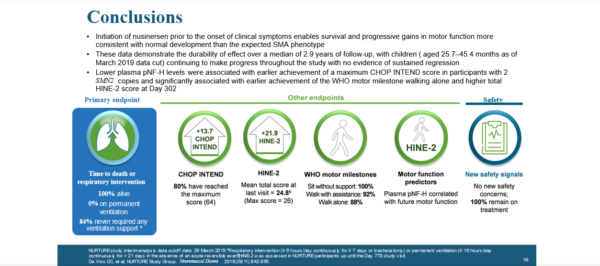
?Все 25 пациентов-участников живы и не нуждаются в постоянной (более 16 часов) вентиляции или трахеостоме
? В респираторной поддержке не более 6 часов в сутки на период не превышающий 7 дней — нуждались 16% больных — т.е. 4 пациента (из группы SMN2=2, т.е. 27% от численности группы). У всех из них потребность в вентиляции возникла на фоне острого инфекционного заболевания
?В респираторной поддержке более 16 часов в сутки или установке трахеостомы на период превышающий 21 день — не нуждался никто.
? Если сравнивать с естественным течением СМА — то по общемировым данным к 13,5 месяцев большинство пациентов — нуждаются в респираторной поддержке длительно
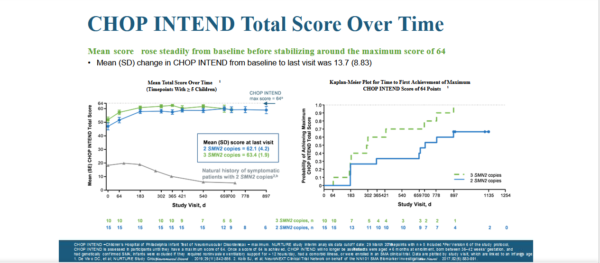
? 80% больных достигли максимального балла оценки моторных навыков по шкале CHOP-Intend
?Оценка моторных навыков по шкале CHOP-Intend — среднее увеличение на 13,7 баллов (прим. но нужно понимать, что все пациенты досимптоматические были на хорошем уровне в начале исследования и фактически это улучшение на баллы приводит к достижению максимального балла по этой шкале — т.е. ограничение метода)
? По шкале HINE-2 средний балл достиг 24,8 (при максимальном 26)
?Обратите внимание на слайд, в котором демонстрируются кривые по ЧОП-Интенд — по натуральной истории (серая кривая внизу) у симптоматических пациентов без лечения и верхние кривые у пресимптоматических на лечении
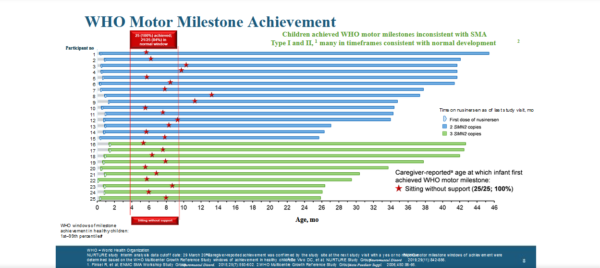
?Уровни моторных навыков по шкалам WHO (ВОЗ):
? Способность самостоятельно сидеть без поддержки — достигли 100% пациентов (25)
?При этом, 21 пациент — в пределах возрастной нормы развития здорового ребенка, 4 ребенка с небольшими задержками (все 4 из группы SMN2=2)
? Способность [ходить с поддержкой — достигли 92% пациентов (23 из 25)
?При этом, 2 пациента не достигли этого навыка на момент среза;
? 15 пациентов достигли этого навыка в пределах возрастной нормы развития здорового ребенка, 8 детей с задержками (7 из группы SMN2=2 и 1 из группы SMN2=3)
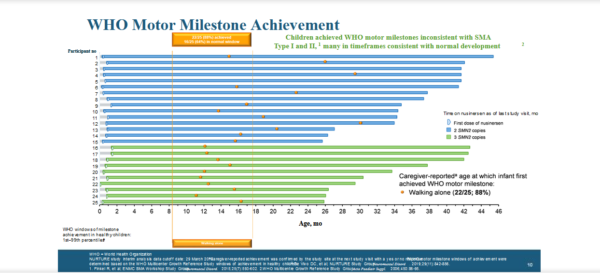
? Способность ходить самостоятельно без поддержки — достигли 88% пациентов (22 из 25)
?При этом, 3 пациента не достигли этого навыка на момент среза;
? 14 пациентов достигли этого навыка в пределах возрастной нормы развития здорового ребенка, 6 детей с задержками (все 6 из группы SMN2=2), при этом важно, что все пациенты из группы SMN2-=3 все достигли этого навыка в пределах возрастной нормы развития здорового ребенка.
?Важно! Обратите внимание на слайдах — в левой части виден возраст начала терапии по каждому пациенту, а также отмечены значками возрастные интервалы развития того или иного моторного навыка.
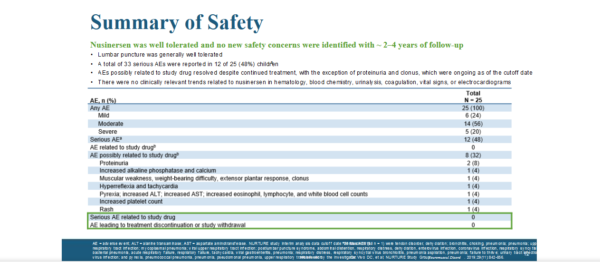
? Побочные эффекты — в целом препарат хорошо переносился, как и люмбальная пункция. Нежелательные явления, выявленные в количестве 33 (за период исследования на момент среза) у 48% пациентов не отличались от тех, что описаны в инструкции по применению препарата и не связаны напрямую с применением самого препарата.
Данный материал носит исключительно информационный характер и не может служить рекламой препарата. Рекомендации относительно индивидуального применения лекарственного препарата следует получать у вашего лечащего врача.
Источник:
Письмо Биоген, обращенное к пациентскому сообществу (перевод)



