В марте 2020 года в научном журнале The Lancet Neurology была опубликована статья «Применение Нусинерсена для лечения взрослых с проксимальной (5q) спинальной мышечной атрофией: наблюдательное, многоцентровое исследование» (авторский коллектив Hagenacker T, et al). В статье представлены результаты независимого исследования реальной практики применения препарата Нусинерсен (торговое наименование – Спинраза) у подростков и взрослых со СМА в 10 клинических центрах Германии.
Описанные результаты наблюдения за эффективностью и безопасностью применения Спинраза показали значительные клинически значимые улучшения моторной функции у взрослых больных СМА, получавших лечение. Эта публикация вносит значительный вклад в понимание значимости терапии у взрослых пациентов, данные о применении терапии у которых ранее были крайне ограничены. На сегодняшний момент – эта публикация содержит результаты наблюдения за самой большой на сегодня когортой взрослых больных со СМА, получавших лечение и вносит значительный вклад в свидетельства, поддерживающие применение терапии Спинраза для взрослых пациентов.
Исследование содержит данные от 124 взрослых больных СМА (в основном, 2 и 3 типов), получавших лечение в 10 нервно-мышечных центрах Германии и основано на оценке двигательных функций с помощью нескольких шкал: Хаммерсмит (HFMSE), RULM и 6-минутного теста ходьбы (6MWT).
Учитывая факт медленного функционального ухудшения состояния у взрослых пациентов со СМА при естественном течение заболевания (без лечения), полученные данные позволяют говорить о том, что лечение взрослых больных со СМА с помощью нусинерсен позволяет достичь значимых клинически улучшений двигательной функции или стабилизации состояния взрослых больных СМА. При этом, не выявлено зависимости и взаимосвязи возраста пациентов и эффективности терапии.
Описание исследования
Несмотря на одобрение применения нусинерсена (Спинраза) для всех групп пациентов, независимо от возраста и типа заболевания большинством регуляторов, однако, данные по эффективности и безопасности применения препарата у взрослых больных со СМА оставались фрагментарными. Единственное ранее опубликованное исследование описывает применение Спинраза у 19 взрослых пациентов со СМА 3 типа и описывает значительное улучшение моторной функции после 300 дней применения нусинерсен.
Исследовательский коллектив поставил целью выяснить безопасность и эффективность применения Спинраза у широкой и разнородной группы взрослых пациентов со СМА. Для этого в наблюдательное исследование были включены 10 нервно-мышечных центров Германии, в которых проходили лечение пациенты от 16 до 65 лет с генетически подтвержденным диагнозом СМА в период с 13 июля 2017 года до 1 мая 2019 года. Все взрослые пациенты, которые получали лечение в этих 10 центрах были включены в исследование. Для оценки результата лечения влючались только пациенты, получавшие лечение в течение, как минимум, 6 месяцев с продолжением наблюдения вплоть до 14 месяцев на терапии.
173 пациента были скринированы для участия в исследовании, из которых 139 (80%) подошли для анализа данных. Из них, 124 пациента (89%) были включены в срез данных 6 месячного интервала получения терапии, 92 пациента (66%) – 10-месячного, и 57 (41%) в 14-месячный анализ. Из анализа были исключены пациенты, для которых отсутствовали данные оценок по шкалам при начале терапии, а также в связи с отказом пациентов от участия (2 человека) и в связи с возникшими побочными реакциями на фоне приема препарата (отказ от продолжения лечения – 2 человека).
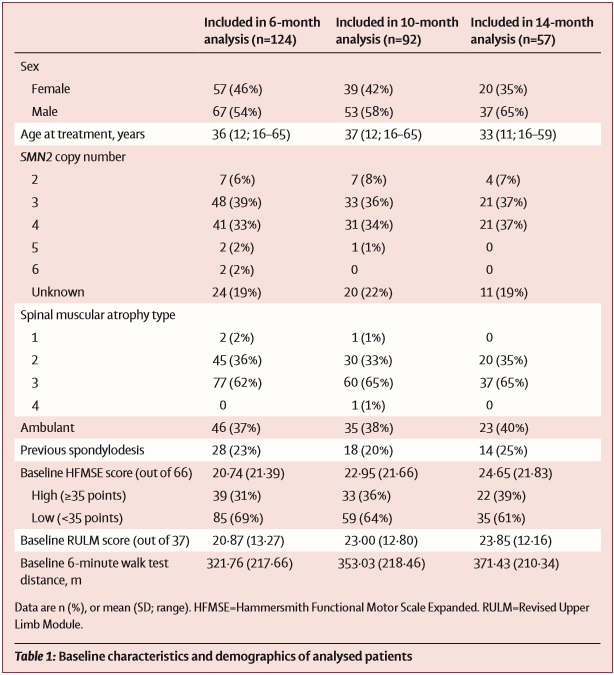
Основные результаты:
Основным инструментом оценки была шкала Хаммерсмит (HFMSE), которая состоит из 33 пунктов оценки моторной функции для оценки повседневной активности. По каждому пункту может быть выставлено от 0 до 2 баллов, таким образом, максимальный балл по данной шкале – 66. Уровень в 3 балла по данной шкале считается клинически значимым.
Средние оценки по шкале Хаммерсмит (HFMSE) значительно повысились по сравнению с оценками перед началом терапии, средняя разница в 6-месячный анализ данных составила 1.73 балла, в 10-месячный – 2.58 балла, в 14-месячный – 3.2 балла.
Клинически значимые улучшения моторной функции (по данной шкале служит отметка в более чем 3 балла) наблюдались у 35 (28%) из 124 пациентов через 6 мес после начала лечения, у 33 (35%) из 92 пациентов через 10 мес после начала лечения, и у 23 (40%) из 57 пациентов через 14 мес после начала лечения.
За исключением 2 пациентов, все пациенты, у который отмечались улучшения более чем в 3 балла по HFMSE к 10 мес с начала лечения – сохранили набранные баллы и к 14-месяцам и далее. У 5 пациентов было установлено улучшение в более чем 10 баллов (3 ходящих и 2 неходячих пациентов со СМА 3 типа с 3 или 4 копиями SMN2, возраст пациентов от 48 до 59 лет). 14 пациентов не смогли показать улучшений на терапии, продолжая ухудшаться. При этом, при анализе не было установлено никакой зависимости от улучшений оценки по HFMSE и возрастом пациентов.
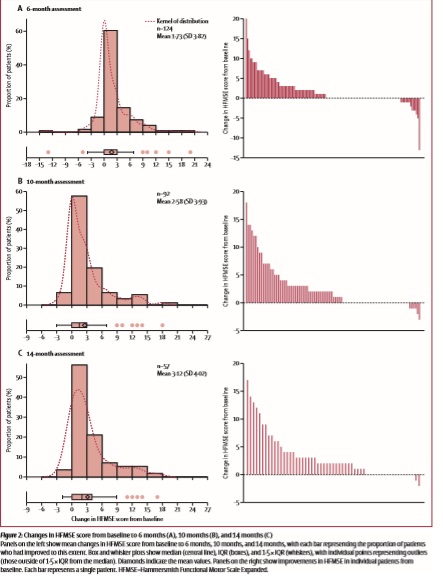
Дополнительно оценивалась функция верхних конечностей по шкале RULM, которая включает 20 разделов, максимально возможное количество баллов по этой шкале – 37, при этом уровень в 2 балла по данной шкале считается клинически значимым.
Функция рук также значительно улучшалась по сравнению с состоянием до начала терапии. Так, у 28 (23%) из 120 пациентов через 6 мес после начала лечения отмечено улучшение функции по шкале RULM как минимум на 2 балла (т.е. клинически значимо), в то время как у 74 (61%) пациентов не отмечено улучшений, у 18 (15%) пациентов отмечалось ухудшение на 1 балл или более, а у 10 (8%) пациентов ухудшение составило 2 балла или более. 28 (23%) пациентов сохранили полную функциональность (37 из 37 возможных баллов на протяжении 6 мес после начала лечения. 21 (75%) пациент из 28 сохранили полную функциональность к 14-месячной отметке после начала терапии. При этом, при анализе не было установлено никакой зависимости от улучшений оценки по RULM и возрастом пациентов.
Также производилась оценка (у ходящих пациентов) по 6-минутному тесту ходьбы (измерение дистанции, которую пациент может преодолеть за 6 минут). Значительные улучшения были установлены у пациентов при анализе после 6-ти, 10-ти и 14-ти мес после начала терапии.
Помимо общего анализа был также проведен дополнительный анализ в разных субгруппах пациентов.
Так, при сравнении групп взрослых пациентов со СМА 2 и СМА 3 типов:
— клинически значимые улучшение по шкале HMFSE (более 3 баллов) были установлены:
у 23 (30%) пациентов из 77 после 6 мес. после начала лечения; 18 (32%) из 60 пациентов после 10 мес.; 15 (41%) из 37 пациентов после 14 мес. лечения в группе больных со СМА3 типа.
У 1 (2%) из 45 пациентов после 6 мес. после начала лечения; 2 (7%) из 30 пациентов после 10 мес.; 1 (5%) из 20 пациентов после 14 мес. лечения в группе больных со СМА2 типа.
— клинически значимые улучшения функции рук по шкале RULM были отмечены на всех трех анализируемых интервалах у пациентов со СМА2 типа, а у пациентов со СМА3 типа только после 14-мес периода наблюдения.
При сравнении групп взрослых пациентов из подгруппы неамбулаторных (неходячих) и амбулаторных (ходячих) улучшения были отмечены во всех временных интервалах у обоих групп, при этом более значительные изменения уровня моторной функции наблюдались в группе ходячих по сравнению с неходячими пациентами.
При сравнении между группами пациентов имеющих перед началом терапии высокий балл по HMFSE (более 35) и низкий балл (ниже 35) было отмечено, что улучшения у пациентов с более высокими изначально баллами были значительнее.
При сравнении групп пациентов с неоперированным позвоночником (96 пациентов) и пациентов с металлоконструкцией в позвоночнике(28 пациентов) – не было отмечено значительного различия в улучшениях баллов по HMFSE. Но при этом отмечается, что эффект от лечения нусинерсен у пациентов с металлоконструкцией был несколько ниже, что, вероятно, связано с предшествующей тяжестью состояния и выражается в более низких баллах HMFSE у таких пациентов до начала терапии.
Безопасность
За 14-месячный период наблюдения не было отмечено каких-либо новых, не выявленных ранее побочных эффектов. При этом, у 82 (47%) пациентов отмечались какие-либо побочные реакции. Наиболее частые побочные реакции на лечение: головные боли у 61 (35%) пациентов, боли в спине 38 (22%) пациентов и тошноту у 19 (11%) пациентов, другие встречались более редко.
Выводы исследования:
Данные, полученные в результате этого исследования показывают значительное улучшение двигательной функции у взрослых пациентов со СМА после начала терапии через 6,10 и 14 мес. После начала терапии. Наибольшее улучшение моторной функции коррелирует с меньшей тяжестью состояния пациента до начала терапии.
В целом, пропорция пациетов со значимым улучшением по шкале HMFSE в группе взрослых пациентов со СМА 3 типа, чем в группе СМА2, но не было установлено никакой корреляции между возрастом пациента и уровнем улучшения моторной функции (т.е. не зависит от времени, прошедшего с момента начала заболевания). А также данные указывают, что более высокий результат показывают пациенты с более чем 35 баллами по HMFSE до начала терапии.
Данные естественного течения заболевания свидетельствуют о том, что взрослые со СМА в среднем ежегодно теряют 0,5-1 балл HMFSE. Конечно, с учетом индивидуальных особенностей пациентов, фазы клинических ухудшений сменяются периодами стабилизации, поэтому эта оценка потери функции – усредненная. Тем не менее, учитывая эти факты, результаты полученные в данном исследовании, подтверждают значительный эффект от терапии нусинерсен у взрослых пациентов.
В части безопасности, не было выявлено никаких не описанных ранее осложнений. Примерно у пятой части пациентов возникали боль в спине и пост-пункционные головные боли, это количество совпадает с общим процентом осложнений при проведении люмбальной пункции (8-25%) в целом.
В исследовании не оценивалось влияние терапии на функцию глотания и дыхания, это потребует дополнительных исследований в будущем. Также дополнительных исследований потребует получение данных наблюдения за долгосрочной эффективностью применением нусинерсен, а также индивидуальых схем применения нусинерсен с учетом режима дозирования и перерывов в лечении.
Данный материал носит исключительно информационный характер и не может служить рекламой препарата. Рекомендации относительно индивидуального применения лекарственного препарата следует получать у вашего лечащего врача.
Источник: The Lancet



