В 2018 году компания Сytokineticsinc.gcs-web.com заявила о результатах испытаний препарата, который потенциально может стать средством лечения для людей со СМА.
Релдесемтив — активатор тропонина быстрых мышц нового поколения, являющийся результатом программы Сайтокинетикс по изучению сокращательной способности скелетных мышц, замедляет высвобождение кальция из регулирующего тропонинового комплекса волокон быстрых скелетных мышц, что приводит к сенситизации саркомера к кальцию, что в свою очередь ведет к повышению сокращательной способности мышц.
Релдесемтив продемонстрировал фармакологическую активность, которая может привести к появлению новых терапевтических возможностей для заболеваний, связанных со слабостью или утомляемостью мышц.
В доклинических моделях СМА активатор скелетных мышц показал повышение субмаксимальной силы скелетных мышц в ответ на нейрональный сигнал и откладывание наступления и облегчение выраженности мышечной усталости. Препарат употребляется перорально (через рот). Более подробно о препарате можно прочитать здесь
Результаты клинических исследований
Результаты 2-й фазы клинических исследований релдесемтива у пациентов со спинальной мышечной атрофией (СМА), проведенных компанией Цитокинетикс, были представлены в 2018 году профессором Джоном В. Дэем (MD, PhD) в ходе презентации на ежегодной конференции Cure SMA в Далласе.
Это исследование, направленное на выдвижение гипотез, достигло и своей основной цели по определению потенциального фармакодинамического эффекта многократного перорального приема релдесемтива у пациентов со СМА, и вторичных целей по определению безопасности, переносимости и фармакокинетики исследуемого препарата.
Цитокинетикс разрабатывает релдесемтив в сотрудничестве с компанией Астеллас как потенциальное средство лечения людей со СМА, а также некоторых других инвалидизирующих заболеваний и состояний, связанных со слабостью и утомляемостью скелетных мышц.
Исследование показало дозо- и концентрато-зависимое увеличение продолжительности времени до утомления мышц через 8 недель после начала приема релдесемтива по сравнению с показателями в начале исследования, что измерялось с помощью 6-минутного двигательного теста (6MW – 6minute walking test), суб-максимального двигательного испытания аэробных возможностей и выносливости, и показателей максимального давления на выдохе (MEP), демонстрирующего силу дыхательных мышц.
В исследовании, в котором испытывались 2 дозы релдесемтива, по 150 и 450 мг 2 раза в день, было выявлено дозозависимое увеличение дистанции, пройденной в ходе 6-минутного двигательного теста у ходящих пациентов, которое измерялось на 2 временных интервалах после начала лечения, через 4 и 8 недель. В группе, принимавшей 150мг релдесемтива 2 раза в день, увеличение дистанции по сравнению с плацебо составило 10.86 метра (p=0.2531) через 4 недели лечения релдесемтивом и 7.72 метра (p=0.4684) через 8 недель лечения. В группе, получавшей 450 мг релдесемтива 2 раза в день, повышение составило 35.63 метра (p= 0.0037) через 4 и 24.89 метра (p= 0.0584) через 8 недель.
Кроме того, была выявлена статистически значимая корреляция между Cmax, или пиковой концентрацией релдесемтива, и повышением показателей 6-минутного двигательного теста с примерным соотношением 9.53 метров/(µg/mL) (p=0.0086).
Помимо этого, исследование показало улучшение показателей максимальной силы на выдохе по сравнению с плацебо. В группе, получавшей 150 мг 2 раза в день, увеличение этого показателя оказалось 5.95 см H2O (p=0.2276) через 4 недели лечения релдесемтивом и 11.69 см H2O (p=0.0378) через 8 недель лечения. В группе, получавшей 450 мг 2 раза в день, рост по сравнению с плацебо был 9.17 см H2O (p=0.0855) через 4 недели лечения релдесемтивом и 13.15 см H2O (p=0.0298) через 8 недель лечения.
Другие показатели, замеренные в ходе исследования, включая Функциональную моторную шкалу Хаммерсмита – Расширенную (HFMSE), Пересмотренный модуль верхних конечностей (RULM), измерение времени на вставание и форсированная жизненная емкость легких, не показали значимых отличий в группе принимающих релдесемтив и в группе принимающих плацебо.
Побочные эффекты
Побочные эффекты в группах релдесемтива и плацебо были одинаковыми. Наиболее часто наблюдаемыми побочными эффектами были головная боль, запор и тошнота. У четырех пациентов были отмечены серьезные побочные эффекты, которые привели ко временному прекращению участия в исследовании, но все они были оценены как не имеющие отношения к релдесемтиву
Данный материал носит исключительно информационный характер и не может служить рекламой. Рекомендации относительно индивидуального применения этого лекарства следует получать у вашего лечащего врача.
Другие статьи о препарате Релдесемтив
Последние публикации о лекарствах и клинических испытаниях

Заявление компании Рош о поддержке пациентов в связи с конфликтом в Украине
10 марта компания Рош в официальном обращении пациентскому сообществу сообщила о продолжении поставок препарата рисдиплам для пациентов в России, а также об открытии специальной программы поддержки доступа к рисдиплам для украинских пациентов СМА, как в Украине, так и вынужденных покинуть страну.

Данные 6-12 месячного наблюдения пациентов в исследовании STRONG интратекального применения AVXS-101
Исследование СТРОНГ стартовало в конце декабря 2017 года. Оно было остановлено FDA в 2019 году после сообщения о находках в параллельных преклинических исследованиях, которые могли потенциально влиять на безопасность применения. После долгих проверок данных это ограничение было снято во второй половине 2021 года, однако прерванный набор в исследование СТРОНГ не возобновился. После снятия ограничений на проведение исследований AVXS-101 IТ (интратекального ввода) были запущены другие, новые программы клинических исследований IT-версии препарата.
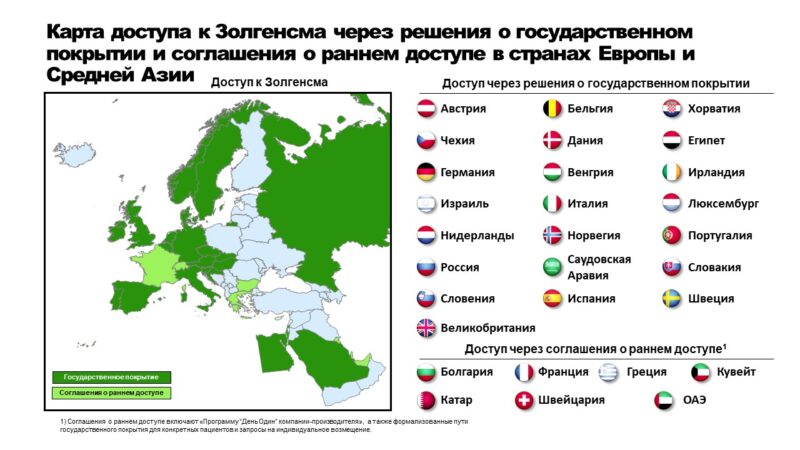
Доступ к Золгенсма в странах Европы и Средней Азии
В России препарат был одобрен в декабре 2021 года и оплачивается за счет средств федерального бюджета в рамках государственного фонда «Круг Добра».
Хирургия позвоночника эффективна у детей со СМА 1 типа, но не лишена рисков
Операция по исправлению кифосколиоза — сочетания двух типов аномального искривления позвоночника — позволяет успешно ввести Спинразу (нусинерсен) в позвоночный канал у детей со спинальной мышечной атрофией (СМА) 1 типа, как показывает исследование серии случаев.

Инструкция к препарату Онасемноген абепарвовек (Золгенсма)
Золгенсма (onasemnogene abeparvovec) — препарат генной терапии, разработанный для лечения больных проксимальной спинальной мышечной атрофией, вызванной нарушением в гене SMN1.

Инструкция к препарату Рисдиплам (Эврисди)
Рисдиплам (Эврисди) – препарат для лечения СМА, разработанный компанией Roche в сотрудничестве с PTC Therapeutics и SMA Foundation. Рисдиплам является модификатором сплайсинга (генетической модификации) гена SMN2, увеличивающим экспрессию полноразмерных функциональных белков.

