Компания Рош сообщает о подаче заявки на регистрацию препарата Рисдиплам в США.
Поданное на регистрацию досье по препарату Рисдиплам включает 12-месячные данные из основных исследований FIREFISH и SUNFISH для широкого круга людей, живущих с типами СМА 1, 2 или 3.
FDA одобрило заявку на регистрацию препарата в ускоренном приоритетном режиме, решение регулятора о возможном одобрении к применению ожидается к 24 маю 2020.

Обозначение «Приоритетное\ускоренное рассмотрение» присваивается лекарственным средствам, которые, по мнению FDA, могут значительно повысить безопасность и эффективность лечения, профилактики или диагностики серьезных заболеваний. Ранее, FDA также предоставило орфанный статус для Рисдиплам в январе 2017 года, а затем «Fast track» (ускоренное рассмотрение) в апреле 2017 года.
«Испытания FIREFISH и SUNFISH были разработаны для представления реального спектра людей, живущих со СМА и включают многих людей, ранее недопредставленных в клинических испытаниях», — сказал Леви Гарравей, руководитель отдела по разработке глобальных продуктов Roche. «Мы рассчитываем на тесное сотрудничество с FDA для того, чтобы как можно более широкий круг пациентов мог получить доступ к препарату».
Представленный пакет документов о рисдипламе включает 12-месячные данные из исследований части 1 FIREFISH и SUNFISH, а также данные из подтверждающей части 2 SUNFISH. FIREFISH.
FIREFISH — это открытое, основополагающее клиническое исследование, состоящее из двух частей, у детей с СМА 1типа. Часть 1 была исследованием увеличения дозы у 21 ребенка в возрасте от одного до семи месяцев. Основная цель части 1 состояла в том, чтобы оценить профиль безопасности рисдиплама у детей и определить дозу для части 2, которая является основным испытанием, оценивающим эффективность рисдиплам у 41 младенца с типом 1 СМА в течение 24 месяцев с последующим продлением применения препарата к открытом исследовании.
SUNFISH — это двойное слепое плацебо-контролируемое клиническое исследование, состоящее из двух частей, у детей и молодых людей (2-25 лет) с типом 2 или 3 СМА. Часть 1 определила дозу для подтверждающей части 2 и оценила эффективность и безопасность препарата. SUNFISH Part 2 — это большое плацебо-контролируемое исследование, оценивающее лечение людей с СМА типа 2 или 3, недавно достигла своей основной конечной точки изменения по сравнению с базовой линией по шкале моторной функциональной меры 32 (MFM-32).
На сегодня, никаких связанных с лечением выводов по безопасности, приводящих к отмене исследования, в каких-либо исследованиях по рисдипламу до настоящего времени не наблюдалось. Безопасность рисдиплама соответствовала его известному профилю безопасности, и никаких новых сигналов безопасности обнаружено не было. Результаты будут представлены на предстоящих медицинских конгрессах.
В случае одобрения Рисдиплам, являющийся сиропом для перорального применения, станет первым лекарством, которое возможно применять на дому для людей, живущих со СМА.
В дополнение к исследованиям, включенным в представленное регулятору досье, Рисдиплам изучается в широкой программе клинических испытаний с пациентами в возрасте от новорожденных до 60 лет, и включает пациентов, ранее получавших другие препараты для лечения СМА.
В конце ноября 2019 года компания Рош в письме к членам сообщества СМА поделилась актуальной информацией о возможной дате регистрации препарата в США. Ожидается, что это случится к 24 мая 2020 года.
Ниже приведен русский перевод письма.
«Уважаемые члены сообщества СМА,
В рамках нашего постоянного партнерства и после вашего запроса на получение своевременной информации о программе клинической разработки препарат рисдиплам, мы рады поделиться с вами тем, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) приняло подачу нашей заявки на регистрацию нового лекарства рисдиплам для применения у людей, живущих со спинальной мышечной атрофией (СМА). FDA предоставило заявке приоритетную проверку в ускоренном режиме, что означает, что агентство рассмотрит заявку в течение 6 месяцев вместо стандартных 10 месяцев. Ожидается, что FDA примет решение об одобрении к 24 мая 2020 года.
Представление регистрационного досье о рисдипламе включает 12-месячные данные из части 1 исследований FIREFISH и SUNFISH, а также данные из подтверждающей части 2 исследования SUNFISH. В дополнение к работе с FDA, мы будем работать с органами здравоохранения по всему миру с целью определения подходящих путей подачи регистрационных заявок для нашего продукта рисдиплам. В Европе мы планируем подать заявку на получение разрешения на маркетинг (MAA) в Европейское агентство по лекарственным средствам (EMA) к середине 2020 года. В обоих регуляторных агентствах мы надеемся получить «широкий лейбл» для лечения СМА у детей и взрослых пациентов. Мы благодарны за возможность сотрудничать с регулирующими органами на протяжении всей нашей программы клинической разработки препарата и во время подготовки к подаче и / или рассмотрению любой заявки.
Достижения в области медицинской науки имеют смысл только тогда, когда они достигают людей, которые в таких разработках нуждаются. Как компания, движимая возможностью улучшения жизни пациентов и семей, которых коснулась СМА, мы очень рады сделать следующий шаг вперед к тому, чтобы сделать рисдиплам доступным для всех пациентов, которые могут получить пользу от лечения.
Мы благодарим всех в сообществе, особенно пациентов и семьи, которые участвуют в наших исследованиях, а также пациентские сообщества во всем мире, которые поддержали и работали с нами для достижения этой вехи. Наше путешествие по разработке методов лечения людей со СМА по-прежнему вдохновлено вами. Мы с нетерпением ждем новых обновлений о нашей программе и поделимся с вами по мере их появления.
Если у вас есть какие-либо вопросы по поводу этого обновления, пожалуйста, не стесняйтесь обращаться ко мне.
Fani Petridis, от имени Глобальной Команды СМА Рош,
Директор по взаимодействию с пациентами, департамент редких заболеваний»
Часто задаваемые вопросы и ответы:
1. Что такое «Приоритетное рассмотрение»?
Назначение «Приоритетное рассмотрение присваивается лекарствам, которые, по мнению FDA, могут значительно повысить безопасность и эффективность лечения, профилактики или диагностики серьезных заболеваний. Ранее FDA в январе 2017 года также присвоило орфанный статус препарату рисдиплам, после чего в апреле 2017 года – «Fast Track» (ускоренное рассмотрение документации).
***
2. Что такое рисдиплам?
Рисдиплам — это исследуемый перорально вводимый жидкий модификатор сплайсинга гена выживаемости мотонейронов SMN-2 для лечения СМА, который изучается у широкого круга пациентов со СМА в возрасте от 1 месяца до 60 лет. Он предназначен для обеспечения устойчивого увеличения белка SMN, который играет важную роль в поддержании специализированных нервных клеток (так называемых моторных нейронов), которые передают сигналы от головного и спинного мозга к скелетным мышцам, позволяя телу двигаться.
Белок SMN можно обнаружить по всему телу, с самыми высокими уровнями в спинном мозге и той части мозга, которая связана с спинным мозгом (ствол мозга). Рисдиплам увеличивает уровень белка SMN как в центральной нервной системе, так и периферически при ежедневном дозировании и в настоящее время проходит оценка его потенциальной способности помогать гену SMN2 вырабатывать более функциональный белок SMN по всему организму.
Компания Рош возглавляет программу клинической разработи рисдиплама в сотрудничестве с SMA Foundation и PTC Therapeutics.
***
- Что такое исследования FIREFISH и SUNFISH?
FIREFISH — это глобальное открытое исследование (тип клинического исследования, при котором все пациенты получают исследуемый препарат и не используется плацебо — вещество, не имеющее лекарственной / терапевтической ценности). Основное исследование, состоящее из двух частей, у детей в возрасте от одного до семи лет месяцев с 1 типом СМА. Часть 1 представляла собой исследование по выявлению оптимальной дозы у 21 ребенка, основной задачей которого было оценить профиль безопасности рисдиплама и определить дозу для части 2. Часть 1 также позволила предварительно оценить эффективность в качестве конечной точки исследования. Часть 2 испытания началась в марте 2018 года и оценивает эффективность и безопасность рисдиплама у 41 ребенка в дозе, выбранной из части 1. Набор пациентов на участие в Части 2 был завершено в ноябре 2018 года, и на сегодня исследование продолжается. Первичный анализ эффективности запланирован на 1 квартал 2020 года.
SUNFISH — это двойное слепое плацебо-контролируемое исследование, состоящее из двух частей (тип клинического исследования, в котором ни участники, ни исследователи не знают, кто проходит курс лечения препаратом или плацебо), — основное клиническое исследование у детей и молодых людей в возрасте от 2 до 25 лет со 2 или 3 типом СМА. Часть 1, в которую входил 51 пациент, определила дозу для подтверждающей части 2 и позволило предварительно оценить эффективность препарата в качестве конечной точки исследования. Основная цель части 2 состояла в том, чтобы оценить моторную функцию, используя общий балл по моторной функциональной шкале 32 (MFM-32) за 12 месяцев. MFM-32 — это проверенная шкала, используемая для оценки двигательной функции у людей с неврологическими расстройствами, включая СМА. SUNFISH часть 2 недавно достигла своей основной конечной точки по изменениям состояния по сравнению с базовой линией по шкале моторной функциональной шкалы MFM-32 после одного года лечения рисдипламом по сравнению с плацебо. До настоящего времени ни в одном исследовании по рисдипламу не было обнаружено никаких данных о безопасности, которые привели бы к выходу из исследования. Безопасность рисдиплама соответствовала его уже известному профилю безопасности, и никаких новых сигналов безопасности обнаружено не было. Результаты будут представлены на предстоящих медицинских конгрессах.
***
- Когда вы планируете подать заявку на одобрение регулирующих органов в Европе и остальном мире?
Различные органы здравоохранения следуют разным процессам и предъявляют разные требования к подаче документов, которые в значительной степени отражают различия в процедуре и сроках рассмотрения каждой заявки.
После предыдущих обсуждений с Европейским агентством по лекарственным средствам (EMA) к середине 2020 года мы планируем представить заявку на получение разрешения на маркетинг (MAA) для рисдиплама. ЕМА указали, что они поддерживают MAA, включая FIREFISH и SUNFISH Part 1 и 2 в первоначальной заявке, чтобы лучше всего поддержать их общий обзор представленных данных.
В то же время мы будем тесно сотрудничать с органами здравоохранения по всему миру с целью определения подходящих путей подачи заявок на регистрацию и обеспечения доступности рисдиплама как можно скорее для всех пациентов со СМА, подходящих для лечения.
***
- Когда вы ожидаете одобрения регулирующих органов?
Если у фармацевтической компании есть доказательства из ее ранних испытаний и доклинических и клинических исследований, что лекарство считается безопасным и эффективным для его предполагаемого использования, компания может подать заявку на регистрацию препарата. После того как фармацевтическая компания подаст заявку, органы здравоохранения сначала проверят поданную заявку и решат, заполнен ли файл (этот процесс иногда называют «валидизацией»). Если заявка заполнена корректно, то процесс оценки и, в конечном итоге, сроки принятия решения о том, может ли быть разрешено использование исследуемого лекарственного средства, зависят от органов здравоохранения, их процедур и сроков. Например, в США процедура FDA имеет от 6 до 10 месяцев (после проверки заявки), чтобы принять решение о том, следует ли утверждать препарат, тогда как в Европе это может занять до 210 рабочих дней. Эти сроки не включают требуемое время ответить на потенциальные вопросы, которые могут быть заданы органами здравоохранения. В результате общее время от подачи до утверждения может быть приблизительно 8-12 месяцев для США (в зависимости от того, применяется ли приоритетное или стандартное рассмотрение заявки) и приблизительно 8-15 месяцев в Европе (в зависимости от того, ускоренная оценка или стандартная оценка).
***
- Когда рисдиплам будет коммерчески доступен в моей стране?
Нормативное одобрение — это только первый шаг к коммерческой доступности. Национальный доступ к исследуемым лекарственным средствам определяется местными властями, которые несут ответственность за предоставление возмещения\оплату терапии в каждой стране, и обычно включает в себя множество дополнительных шагов. Таким образом, сроки национального возмещения могут существенно различаться в разных странах, и, в настоящее время мы не можем дать достоверную информацию на этот счет. Рош активно сотрудничает с органами здравоохранения, правительственными учреждениями и другими ключевыми заинтересованными сторонами во всем мире с целью обеспечения широкого и быстрого доступа к рисдипламу для всех пациентов, которые могут получить пользу от лечения.
***
- Будет ли возможно получить доступ к рисдиплам до одобрения, на основе программ сострадательного применения (compassionate use)?
Мы понимаем срочность удовлетворения потребностей и повседневных сложностей людей со СМА и их семей, их беспокойство по поводу доступа к исследуемым лекарствам как можно скорее.
Нашей основной целью является проведение необходимых клинических исследований для получения медицинских данных, которые будут позволят достичь одобрения препарата и возмещения расходов на лечение со стороны регулирующих органов.
На данном этапе мы планируем внедрить рисдиплам через программу предварительного одобрения доступа (Pre-Approval Access — PAA) (ППОД) или для сострадательного применения (compassionate use — CU) (ПСП). Мы изучаем возможность запуска таких программ с органами здравоохранения. Поскольку механизмы PAA / CU (ППОД\ПСП) для новых лекарств различаются в разных странах, могут возникнуть различия в программе и сроках. В конечном итоге мы продолжим работать с органами здравоохранения и надеемся предоставить пациентам рисдиплам в качестве лицензированного продукта как можно скорее. Мы обязуемся возвращаться к сообществу и делиться последними новостями как только информация станет доступна.
Для получения дополнительной информации о критериях программ до одобрения препарата, пожалуйста, обратитесь к «Позиции Рош по предварительному одобрению доступа к исследуемым лекарственным средствам» на официальном веб-сайте Roche:
***
- Клинические исследования рисдиплама все еще набирают участников? Где я могу получить дополнительную информацию об исследованиях по рисдипламу, в которые открыт набор?
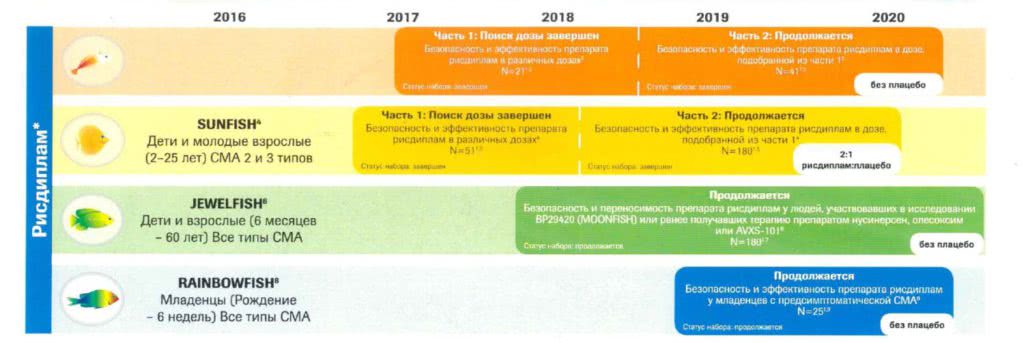
Есть два испытания рисдиплама, JEWELFISH и RAINBOWFISH, где в настоящее время продолжается набор участников. JEWELFISH будут набирать участников до конца 2019 года, тогда как в RAINBOWFISH только начали набор. На веб-сайте clinicaltrials.gov перечислены текущие и прошедшие клинические испытания, в том числе информация о состоянии исследования и о том, проводит ли оно набор пациентов. Если вы введете в поиск на сайте «Spinal Muscular Atrophy», вы сможете найти информацию обо всех зарегистрированных клинических исследованиях по СМА. Информацию о двух испытаниях можно найти по адресу:
Мы рекомендуем вам поговорить со своим врачом о том, что может быть лучшим вариантом для вас.
***
- О программе клинической разработки рисдиплам
Программа клинической разработки рисдиплама Рош сосредоточена вокруг четырех многоцентровых исследований, призванных помочь нам понять, как лекарство может влиять на широкий спектр людей, живущих со СМА. Мы оцениваем безопасность и потенциальную пользу рисдиплама у пациентов со СМА в диапазоне от младенцев до проявления первых симптомов до 60 лет, а также у пациентов, ранее получавших другие виды терапии.
Данный материал носит исключительно информационный характер и не может служить рекламой препарата. Рекомендации относительно индивидуального применения лекарственного препарата следует получать у вашего лечащего врача.
Источник: Сайт Roche



